Por Agencia Xinhua
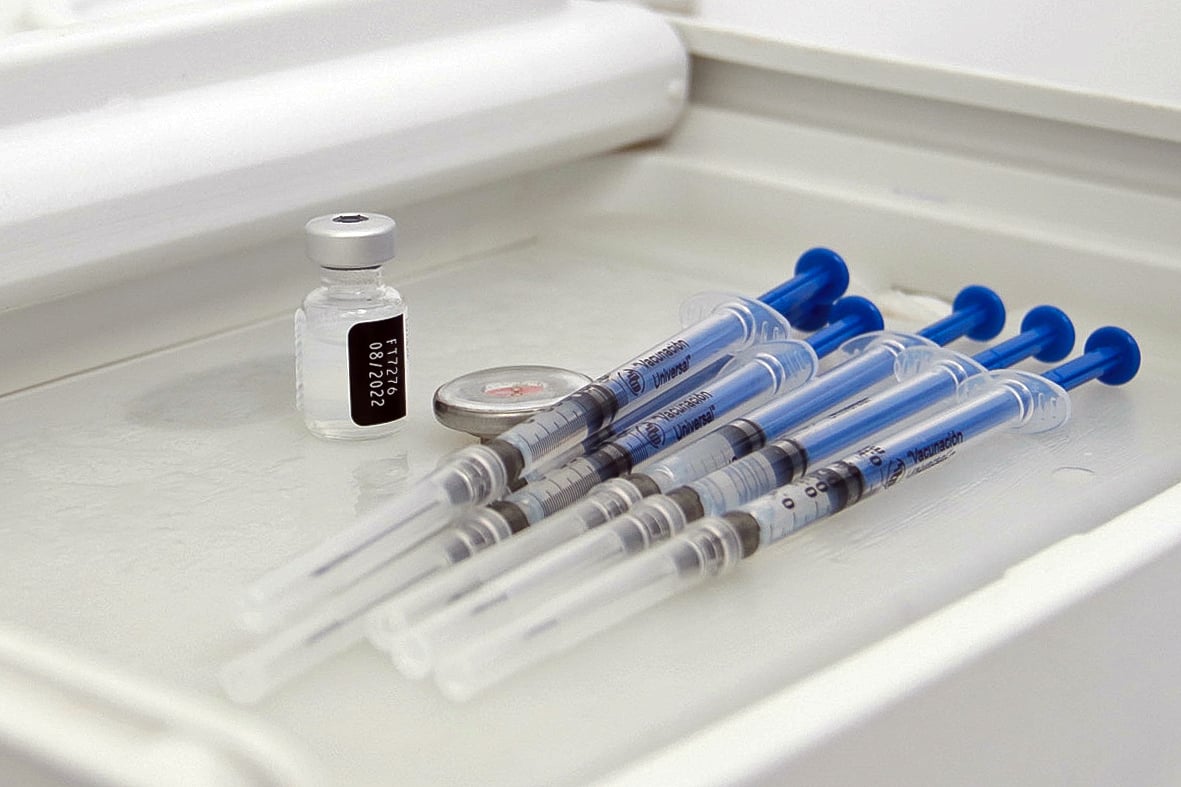
Los Ángeles. La Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) autorizó el uso de emergencia de las vacunas de Moderna y Pfizer-BioNTech contra la covid-19 para niños de seis meses en adelante.
Para la vacuna de Moderna, la FDA enmendó la autorización de uso de emergencia para incluir el uso de la vacuna en individuos desde seis meses hasta 17 años. La vacuna había sido previamente autorizada para su uso en adultos de 18 años en adelante.
En cuanto a la vacuna de Pfizer-BioNTech, la FDA enmendó la autorización de uso de emergencia para incluir el uso de la vacuna en individuos de seis meses a 4 años. La vacuna ya había sido autorizada con anterioridad para su uso en individuos de 5 años o más.
La FDA dijo que su evaluación y análisis de los datos de seguridad, efectividad y manufactura de estas vacunas fue rigurosa e integral y apoya las autorizaciones de uso de emergencia.
Razones de la FDA
La agencia determinó que los beneficios potenciales y conocidos de las vacunas de Moderna y Pfizer-BioNTech contra la covid-19 superan los riesgos potenciales y conocidos en las poblaciones pediátricas autorizadas para cada vacuna.
La decisión de la FDA se produce después de una reunión de sus asesores realizada esta semana, en la que votaron a favor de recomendar las vacunas de Moderna y Pfizer-BioNTech contra la covid-19 para niños desde seis meses de edad.
Foto: Agencia Enfoque
Recuerda suscribirte a nuestro boletín
📲 bit.ly/2T7KNTl
📰 elciudadano.com